
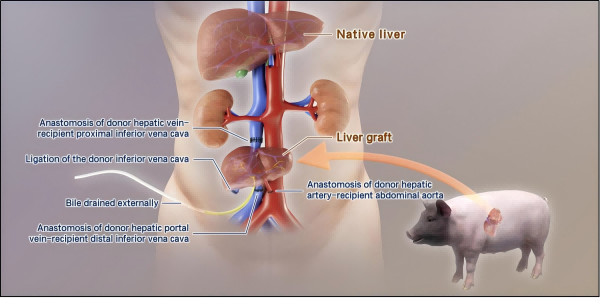
图 猪-人异种肝移植示意图
在国家自然科学基金项目(批准号:82325007、82371793、82070671、82170667)等资助下,第四军医大学西京医院窦科峰教授、王琳教授、董海龙教授团队在异种肝移植方面取得进展,研究以“基因编辑猪-人肝移植(Gene-modified pig-to-human liver xenotransplantation)”为题,于2025年3月26日在《自然》(Nature)杂志上在线发表。论文链接为:https://www.nature.com/articles/s41586-025-08799-1。
全球范围内,终末期肝病患者面临着供体器官严重匮乏的生存困境。作为解决器官短缺的创新方案,基因编辑猪异种移植技术已取得新的进展,继心脏、肾脏成功完成人体移植后,我国科研团队在异种肝移植领域取得重要研究成果。
本研究采用六基因编辑猪(沉默猪源性免疫排斥基因及表达人源性免疫耐受基因)为供体肝源,移植受体为脑死亡患者,术后进行了为期十天的观察监测。在移植前证实供体猪外周血单核细胞和肝组织中致超急性排斥反应的GGTA1、B4GALNT2和CMAH基因已失活,人源补体调节蛋白CD46/CD55以及抗血栓蛋白TBM显著过表达。异位辅助肝移植术中精准匹配血管尺寸,将供肝的肝静脉和门静脉接入受体的下腔静脉系统,将供肝的肝动脉与腹主动脉吻合,并建立胆汁外引流。术后超声显示肝动脉血流速度稳定于41.45~60.63 cm/s,门静脉血流参数正常。移植后供肝立即出现胆汁分泌,猪源白蛋白水平显著上升;直至观察终点,谷草转氨酶虽有短暂升高,但谷丙转氨酶、碱性磷酸酶等核心指标维持正常,凝血功能总体稳定且波动在生理范围内。补体活化、细胞及体液免疫反应均得到有效抑制。研究中未发现猪内源性逆转录病毒及巨细胞病毒的跨物种传播。该研究表明通过供体猪的六基因编辑策略联合受体的特异性免疫抑制方案,可成功控制异种肝移植的超急性和急性排斥反应,使猪源肝脏在人体内发挥一定的生理功能替代能力(图)。
该研究展示了异种器官移植领域的重要成果,为异种肝移植的临床应用奠定了基础,也为治疗急性肝功能衰竭或等待同种肝移植患者的生命维持提供了干预新思路。