
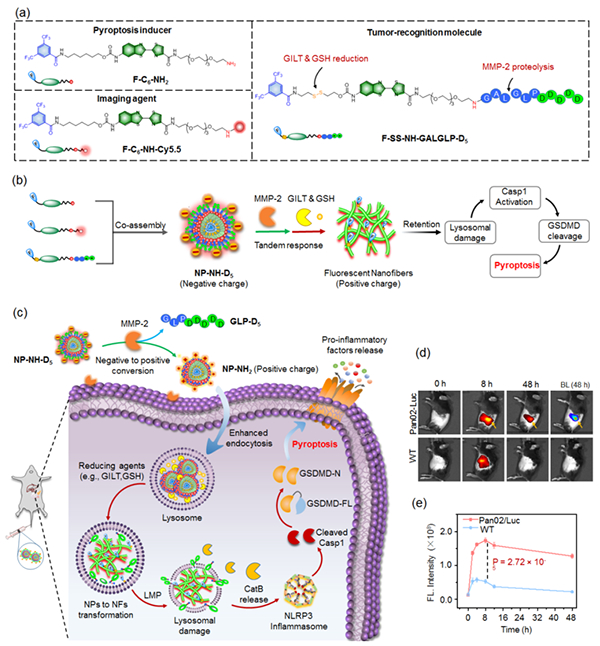
图 (a-c)可级联响应肿瘤微环境的分子组装探针及其研究示意图; (d,e)小鼠模型上原位胰腺癌的荧光成像与信号强度变化
在国家自然科学基金项目(批准号:22274074、2137003)等资助下,南京大学叶德举团队在分子探针活体研究方面取得新进展。相关研究成果以“串联调控溶酶体内组装纤维探针用于活体成像与肿瘤免疫治疗”(Tandem-controlled lysosomal assembly of nanofibres induces pyroptosis for cancer immunotherapy)为题,于2025年2月18日发表在《自然·纳米技术》(Nature Nanotechnology)期刊上。论文链接: https://doi.org/10.1038/s41565-025-01857-9。
分子探针是实现生物分子精准探测与调控的关键工具,广泛应用于疾病诊断、靶标验证、药物研发和分子机制研究等领域。然而,活体内复杂的生物组织屏障、高度动态的环境以及大量干扰物的存在,导致探针的特异性和靶组织递送效率受限,这给当前活体复杂环境中生物分子的精准探测与调控带来了极大困难。
针对上述挑战,该团队通过分子的模块化设计与分子间组装的精确调控,结合表面电荷翻转和结构形貌转变策略,构建了一种可级联响应肿瘤微环境的分子组装探针(NP-NH-D5)。该探针能够在肿瘤微环境中依次识别胞外MMP-2酶和胞内还原性生物分子(GILT酶和谷胱甘肽),并逐级激活,调控探针的表面电荷、尺寸和结构,从而实现高效肿瘤细胞靶向递送。这一过程有效增强了探针在肿瘤的摄取效率,并显著延长瘤内滞留时间,从而增强肿瘤成像信号,实现了小鼠模型中原位及远端转移肿瘤灶的精确定位。
在此基础上,上述团队还进一步探究了探针在肿瘤细胞内的“靶向-组装-破坏-激活”级联过程,阐明了原位组装纳米纤维结构通过快速破坏肿瘤细胞溶酶体,激活GSDMD依赖性的细胞焦亡分子机制。这为活体复杂环境中肿瘤灶的精准定位与靶向免疫治疗提供了一种创新化学策略。