
图2 TMJ-OA髁突神经血管化作用机制及靶向阻断策略示意图
在国家自然科学基金项目(批准号:82471000、82170978、82325012)等资助下,中国人民解放军第四军医大学焦凯教授团队在颞下颌关节神经调控机制研究方面取得进展,系列研究成果连续发表两篇论文:(1)以“交感-感觉神经交互作用对颞下颌关节骨关节炎疼痛的调控机制(Effect of regional crosstalk between sympathetic nerves and sensory nerves on temporomandibular joint osteoarthritic pain)”为题,于2025年1月7日发表在《国际口腔科学杂志(英文版)》(International Journal of Oral Science)杂志。原文链接:https://www.nature.com/articles/s41368-024-00336-6;(2)以“双响应水凝胶通过抑制神经血管化减缓骨关节炎进展(Neurovascularization inhibiting dual responsive hydrogel for alleviating the progression of osteoarthritis)”为题,于2025年2月6日发表在《自然•通讯》(Nature Communications)杂志。原文链接:https://www.nature.com/articles/s41467-025-56727-8。
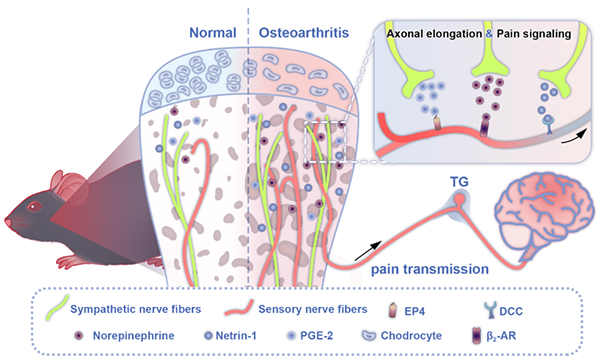
颞下颌关节骨关节炎(temporomandibular joint osteoarthritis,TMJ-OA)是重症颞下颌关节紊乱病患者的主要表现,可导致持续性口颌面部疼痛与关节功能受限,当前治疗手段虽能短暂缓解疼痛,但无法阻断疾病进展,亟需深入解析其病理机制并开发新型干预策略。研究团队通过构建TMJ-OA疼痛模型,发现髁突软骨下骨中交感神经通过释放去甲肾上腺素(NE),协同激活netrin-1和前列腺素E2(PGE2)等神经活性因子,诱导感觉神经异常生长与活化,进而加剧疼痛信号传导,表明颞下颌关节作为“神经性关节”更易受到外周神经的调控和支配(图1)。在此基础上,研究团队发现软骨下骨中带负电的细胞外核酸(exRNA)可通过募集VEGF、Netrin1等正电蛋白,形成核酸-蛋白聚集体,驱动神经血管侵入骨软骨交界区,进而揭示TMJ-OA髁突神经血管化的分子机制。针对这一机制,团队提出双重阻断策略:特异性清除髁突局部exRNA,并持续释放贝伐单抗以抑制VEGF功能。实验表明,该策略可有效阻断神经血管信号通路,抑制异常血管生成,同步改善疼痛行为学指标并促进软骨-骨界面结构再生(图2)。
系列研究从神经调控角度深化了对TMJ-OA病理机制的理解,提出的“神经性关节”理论为同时实现TMJ-OA症状干预和病变阻断提供了潜在新靶点。