
目前,乳腺癌在我国仍位居女性肿瘤的首位,严重危害着我国女性的生命健康,因此也被称为女性健康的“第一杀手”。尽管乳腺癌的发病率较高,但大多数患者的预后情况相对乐观,除了最为棘手的亚型——三阴性乳腺癌。
三阴性乳腺癌(TNBC)以雌激素受体(ER)、孕激素受体(PR)和人表皮生长因子受体2(HER2)的缺失为特征,占所有浸润性乳腺癌的15-20%,并与早期复发和高死亡风险相关。辅助蒽环类/紫杉烷类化疗是早期三阴性乳腺癌的标准治疗,但约20-40%的患者会出现疾病复发。因此,迫切需要更有效的策略来优化三阴性乳腺癌的辅助治疗。
2024年10月23日,复旦大学附属肿瘤医院的邵志敏教授、王中华教授和江一舟教授领导的团队在顶级医学期刊《BMJ》(IF=93.6)上发表了题为“Intensive chemotherapy versus standard chemotherapy among patients with high risk, operable, triple negative breast cancer based on integrated mRNA-lncRNA signature (BCTOP-T-A01): randomised, multicentre, phase 3 trial”的研究论文。
该研究探讨了多基因标记在可手术三阴性乳腺癌患者中定制辅助化疗的可行性,
研究成果证实:基于肿瘤医院自主研发的“多基因模型”,针对三阴性乳腺癌,采用“蒽环紫杉”序贯“吉西他滨”联合“卡铂”的精准治疗方案,让高危患者生存率显著提升超过10%,改变了传统三阴性乳腺癌辅助化疗“千人一方”的局面。

2015年,复旦大学附属肿瘤医院的邵志敏教授和江一舟教授团队基于全转录组表达谱,自主研发构建了一个由5个RNA组成的三阴性乳腺癌预后预测模型(简称“多基因模型”)。
这是国际上首个三阴性乳腺癌预后预测模型,相关研究成果发表于《Cancer Research》。
为了进一步验证“多基因模型”的预后效果并挖掘其临床应用价值,邵志敏教授带领团队开展了名为“BCTOP-T-A01”的临床研究。该研究历时7年,从2016年1月3日至2023年7月17日,共纳入504名18-70岁的早期(M0)三阴性乳腺癌患者。这些患者均在复旦大学附属肿瘤医院接受了单侧浸润性乳腺癌手术,且既往未接受过新辅助治疗。研究对象包括淋巴结阳性和淋巴结阴性但肿块大小超过1厘米的患者。
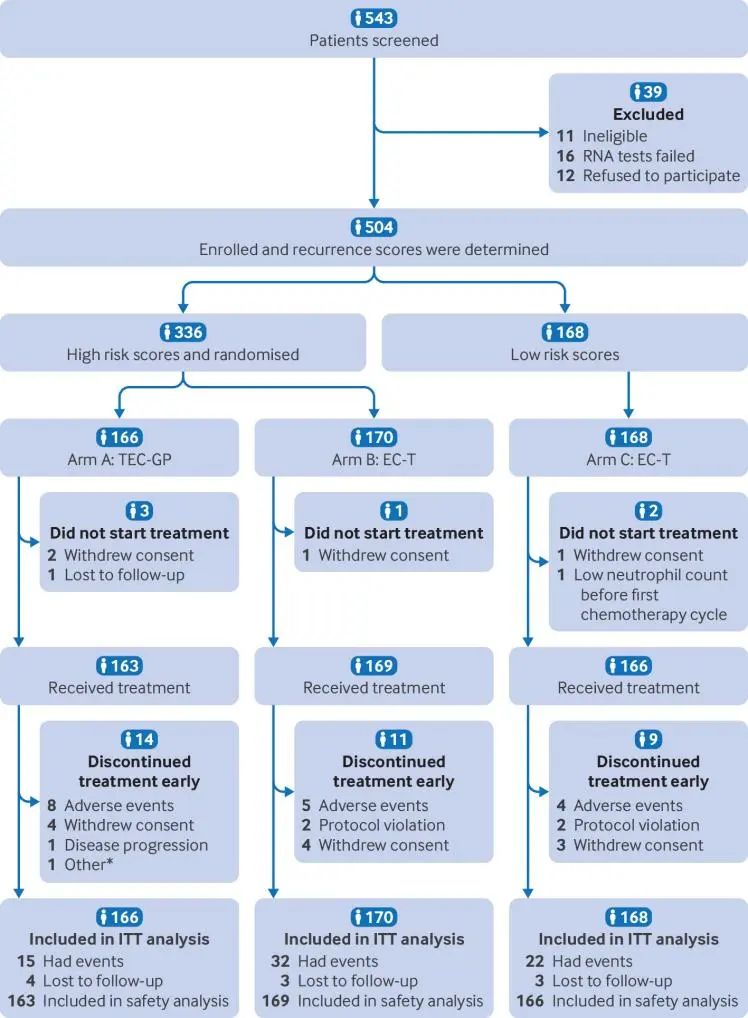
通过预测模型将三阴性乳腺癌患者划分为高危和低危复发风险组,中位随访时间为45个月。
高危患者随机(1:1)分为两组:
A组:强化治疗,包括4个周期的多西他赛、表阿霉素和环磷酰胺,随后4个周期的吉西他滨和顺铂(n=166)。
B组:标准治疗,4个周期的表阿霉素和环磷酰胺,随后4个周期的多西他赛(n=170)。
低危患者接受与B组相同的辅助化疗(C组; n=168)。
主要终点:A组与B组的无病生存率。
次要终点:C组与B组的无病生存期、无复发生存期、总生存期和安全性。
高危患者3年生存率提升10.3%
研究结果显示:无病生存率:A组3年无病生存率为90.9%,B组为80.6%。
无复发生存率:A组3年无复发生存率为92.6%,B组为83.2%。
总生存率:A组3年总生存率为98.2%,B组为91.3%。
低风险组(C组):。低风险组的3年无病生存率(90.1%对比80.6%)、无复发生存率(94.5%对比83.2%)和总生存率(100%对比91.3%)均优于接受相同标准化疗方案(B组)的高危患者。

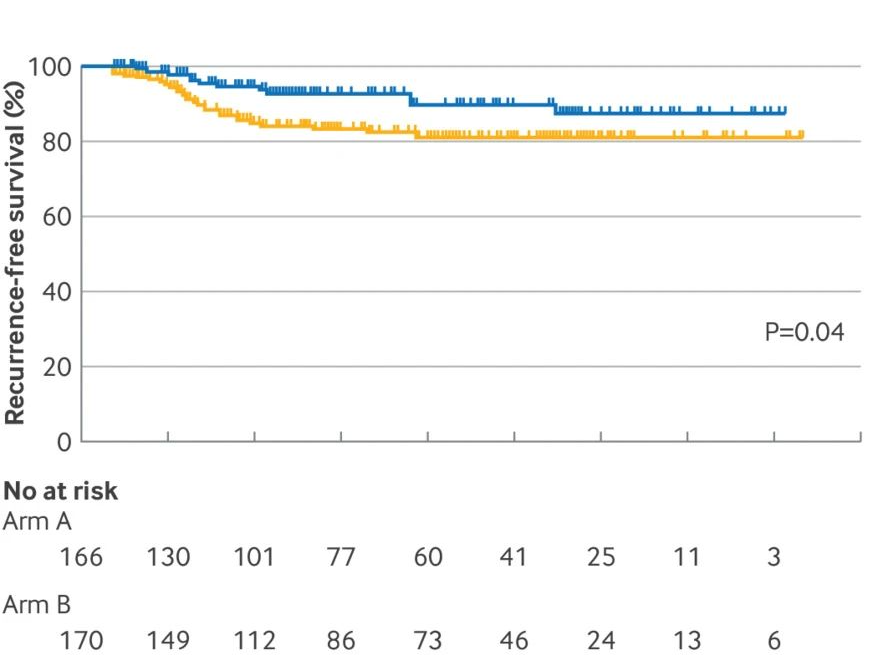
此外关于安全性的探索:
A组、B组和C组分别有8例(5%)、5例(3%)和4例(2%)患者因毒性而停止研究治疗。在接受研究治疗的随机化患者中,A组≥3级治疗相关不良事件的发生率显著高于B组,但A组和B组之间治疗相关严重不良事件或导致停药的治疗相关不良事件的发生率无显著差异。研究中未发生治疗相关死亡。
综上所述,多基因模型指导的精准化疗方案显著提升了高危患者的生存率,超过10%,同时也将低危患者的生存率提高了近10%,有力地证明了该模型的应用价值。
“显著提升高危三阴性乳腺癌患者预后的同时,该治疗方案安全性可控,患者无严重不良反应,体现出该方案的更多优势。”复旦大学附属肿瘤医院乳腺外科主任兼大外科主任邵志敏教授说。

江一舟教授表示,“BCTOP-T-A01”是邵志敏教授牵头成立的乳腺癌精准治疗协作组(BCTOP)开展的首个临床研究。多中心合作模式和取得的重大成果,充分证明了BCTOP成立的宗旨——“基于精准医学理念,开展多中心临床研究,推广转化研究平台,开发新型药物和技术,最终提高我国乳腺癌的诊治水平和国际地位。”
据悉,肿瘤医院正准备开展针对模型预测的低危三阴性乳腺癌患者的降阶梯治疗。相信未来,“BCTOP”会为全球带来更加优质的“中国方案”,造福更多的乳腺癌患者。