
土拨鼠(marmotamonax,英文名称Groundhog)也称为土拨鼠。土拨鼠的平均体重为4.5kg,*大为6.5kg,长度约为56cm。陆地松鼠主要分布在加拿大和其他地区的北美大平原,与松鼠,海狸和花栗鼠一样属于啮齿动物科。动物乙型肝炎病毒包括土拨鼠肝炎病毒(仅在美国东北部东部感染土拨鼠的WHV),地松鼠肝炎病毒(GSHV)和北极松鼠肝炎病毒(ASHV)包括在内。测序表明,WHV和GSHV病毒的核苷酸和氨基酸序列差异非常小,变异程度不大于人类HBV亚型之间的序列变异性。伍德查克模型也是HBV研究中使用*广泛的模型,因为WHV和HBV的基因组组织比禽类肝炎病毒更相似,因此可以在天然宿主中研究整个病毒生命周期。土拨鼠肝炎病毒是一种自发感染东方土拨鼠的病毒。
该病毒于1977年在费城的佩罗斯公园(Perros Park)首次发现,可在伍德查克(Woodchuck)引起慢性肝炎和肝癌。 ..目前,已分离出几种WHV病毒株,它们的基因型相对接近,但是感染新生儿土拨鼠会引起不同程度的慢性肝炎。伍德查克肝炎模型是研究HBV感染和抗病毒治疗中使用*广泛的模型之一。
康奈尔大学(Cornell University)在1980年将Marmot小组提升为实验室模型。初始模型研究进展包括:经过实验感染的成年和少年土拨鼠正在进行肝癌的病毒学和自发研究。自1988年以来,新的Woodchuck WHV模型已开始用于检测针对病毒感染的核苷酸类似物。

早期的研究还测试了针对成人和新生儿土拨鼠急性和自限性WHV感染的传统抗病毒疫苗,并使用土拨鼠模型对新免疫的土拨鼠进行免疫,并测试该疫苗对慢性肝炎和肝癌的预防作用。使用免疫抑制剂环孢菌素A研究急性和慢性感染的免疫调节,并确定宿主免疫系统在WHV感染的自我限制和慢性转化中的作用。自1980年代以来,对土拨鼠肝炎病毒的研究主要集中在模型的建立和应用上,包括病毒感染和疾病的病理学,抗病毒药物筛选以及个体或全身免疫调节。
它是主要内容如下:
(1)WHV感染和疾病的自然发病率:土拨鼠肝炎病毒模型是研究乙肝病毒感染的研究人员广泛接受的模型。*近有关土拨鼠对WHV感染的反应的研究揭示了WHV感染的一系列免疫机制。土拨鼠病毒感染的免疫标记与人类和小鼠的并不完全相同。然而,在土拨鼠感染的过程中,免疫反应的类型和强度与人类乙型肝炎病毒感染的过程非常相似。用WHV感染成年或新生的土拨鼠会使相应的急性感染成为自限性感染,并发展为两种类型的慢性感染,这与人类年龄对HBV感染后果的影响有关。我在做当成年查克感染WHV后,大多数人会自愈,约5%的人会患上慢性肝炎。
然而,在病毒接种和成年土拨鼠急性感染期间,由于环孢菌素A暂时抑制细胞介导的免疫力,因此92%的感染可发展为慢性携带者。仅在疫苗接种期间和急性感染的早期(0-4周)内注射环孢菌素A,并且50%的感染在慢性携带者中发展。
大多数慢性WHV感染是由新生儿获得性感染引起的。新生儿土拨鼠病毒感染可以以60%至75%的速度发展为慢性携带者,其中25%至40%可以自发恢复。在春季感染草原犬鼠时,病毒载量与宿主的免疫反应一致,因此第二年收集的样本可用于数据建模以分析血清学和肝脏变化。这些特征还允许该模型用于在自我限制之前的急性感染期间同时检测宿主反应,以及转化为慢性感染后的血清学特征。因此,有可能识别和区分引起自限性和慢性感染的机制。
慢性WHV感染可引起病毒长期复制,从而导致慢性肝病和肝癌。患有慢性WHV感染的土拨鼠不会自发地从血清中的e抗原转移至e抗体,并逐渐减少病毒复制。这在人类乙型肝炎感染中更为常见。一般而言,慢性WHV在土拨鼠中携带大量病毒复制,非常高的表面和e抗原负荷对于维持宿主对慢性肝病至肝癌的免疫耐受性至关重要。是。自我限制的WHV感染可基本上抑制病毒复制,并完全消除体内的病毒。但是,在自我修复的土拨鼠中,在肝脏,血清和外周单核细胞中检测到痕量的WHV基因组,这可能是另一种持续性感染。同样,被HBV感染后自愈的人可以检测到HBV DNA痕迹。与血清阴性(未感染WHV)的土拨鼠相比,土拨鼠在感染后能够自愈,但仍有5-20%的机会患上肝癌。但是,与长期感染的土拨鼠相比,这种可能性已经非常低(后者为100%)。该结果可以比较慢性WHV与慢性HBV患者和肝癌引起肝癌的现象。
*近,一些学者已经使用CsA抑制免疫系统对感染WHV的土拨鼠的反应,研究WHV病毒复制的激活,并研究具有WHV DNA或病毒抗原的木材。我们发现查克保留在肝脏和外周血中。在CsA治疗期间可以看到WHV的短期恢复,这可能是因为该病毒被宿主的病毒特异性免疫反应所抑制,并保持了低水平的复制。宿主细胞免疫应答的长期记忆与低水平的病毒复制之间的相互作用对于长期稳定地控制病毒复制和抑制感染过程,从而维持恢复期非常重要。对于慢性HBV或WHV感染的抗病毒或免疫治疗,请参阅自发感染的恢复期免疫状态。
(2)病毒分子生物学研究:WHV属于肝炎和原发性肝炎家族。 WHV的遗传组成与HBV和其他哺乳动物肝病毒相似,具有基本相同的生物学特性和复制策略。在感染了WHV的土拨鼠血清中,包膜蛋白(WHsAg表面抗原)构成线性或球形颗粒,完整病毒颗粒的直径为42-45m。该病毒包含核蛋白或核心蛋白(WHcAg)和DNA基因组。 WHV和HBV的复制周期相同。在一些研究中,将WHV基因组克隆,消化,环化成超螺旋DNA,然后注入实质土拨鼠肝中,引起WHV感染。乙肝病毒侵袭肝细胞的感染过程机理尚不清楚。研究表明,大包膜蛋白的S1前区中的某些序列可能负责病毒和细胞相互识别的全部或部分,但到目前为止肝细胞受体尚未完全鉴定。但是,使用单克隆抗体进行的体内中和研究越来越多地揭示了包膜蛋白其他部分的识别位点,仅由小包膜蛋白制备的疫苗就可以发挥有效的保护作用。病毒进入细胞后,部分双链环状DNA进入细胞核,并通过与病毒颗粒连接的内源逆转录DNA聚合酶转化为完整的双链DNA,从而形成完整的双链DNA。是共价闭合的环状cccDNA。在细胞中RNA聚合酶II的作用下,cccDNA充当病毒mRNA转录的模板。将mRNA转录本(略大于病毒基因组)整合到病毒聚合酶和成熟的核心抗原颗粒中,并且病毒聚合酶的RNA依赖性DNA聚合酶活性可催化负转录。
然后,病毒利用其自身的DNA依赖性DNA聚合酶活性合成正链DNA负链长度的约50%至75%。在成熟的WHV和HBV病毒颗粒中发现了这种未封闭的环状双链DNA。包膜蛋白在细胞的内质网中合成,成熟病毒颗粒从肝细胞中释放出来。乙肝病毒本身对受感染的细胞无毒。在HBV中,大多数核心抗原免疫染色发现在细胞核中,而在WHV中,大多数核心抗原染色发现在细胞质中而不在细胞核中。这表明新合成的细胞质核心抗原负责逆转录,部分或全部正链DNA合成,并偶尔重新进入细胞核以合成cccDNA。在HBV中,细胞质中的核心抗原低于检测水平(免疫染色),核抗原的密集染色表明核心抗原现已成熟。然后,成熟的核心抗原通过另一种细胞途径到达内质网,组装表面抗原。在已建立的伍德查克慢性WHV感染模型中,与人类HBV慢性携带者相比,WHV颗粒的浓度是后者的10至100倍。这可能与两者之间核心抗原的不同免疫定位有关。在WHV复制周期中,DNA到RNA的转录过程类似于逆转录病毒,但是DNA没有整合到宿主的基因组中。感染的肝细胞中的游离cccDNA是稳定的,需要从系统中清除感染的细胞,这使其成为宿主乙型肝炎病毒清除的主要目标之一。乙型肝炎病毒DNA进入细胞基因组后,必须将其截短并重新排列,并且可以将其插入细胞基因组中的任何位置,这对于肝细胞的转化至关重要。肝脏的形态学和病毒学研究发现,在感染了WHV的土拨鼠中,有100%的肝细胞被该病毒感染。尽管急性感染消退时会除去病毒中间体,但在病毒复制停止后很长一段时间内,cccDNA仍然存在。
(3)免疫学研究:新生儿和成年土拨鼠感染WHV后,其恢复需要针对肝脏和周围环境中的病毒进行特异性免疫反应以清除病毒。自然恢复过程是慢性感染抗病毒或免疫疗法的基准。许多研究表明,诱导特定的细胞和体液免疫反应是成年患者清除HBV的先决条件。在大多数情况下,与人类患者相比,HBV感染后没有明显的临床症状。因此,尚未详细研究成人的HBV潜伏期和急性期免疫应答的发展及其对感染的影响及其在消除感染中的作用。尽管通常将乙型肝炎病毒认为是乙型肝炎病毒,但可以在除肝脏以外的组织中检测到乙型肝炎病毒DNA。 DHBV可以在鸭胰腺中复制。 HBV和WHV可以感染淋巴系统,目前尚不了解这种现象。一些研究表明,甚至在感染肝之前,WHV就会在淋巴组织中复制和扩散。使用脂多糖刺激携带慢性WHV的土拨鼠外周血单核细胞可以激活其中的静态DNA并形成复制中间体。脂多糖刺激土拨鼠外周血单核细胞的无细胞上清液,这些上清液携带慢性WHV,可感染敏感的成年土拨鼠并引起急性感染。淋巴组织的WHV基因组是处于静态还是复制状态取决于宿主淋巴细胞的状态,包括休眠,分裂,血液和淋巴组织中的循环。在新生土拨鼠感染WHV后一个月,在骨髓中检测到WHV DNA,但是在急性复制阶段,外周血单核细胞,淋巴结和脾脏中出现了WHV的早期复制标记。感染后恢复期间,淋巴组织WHV复制趋于稳定(或完全消除)。在慢性感染中,外周血单核细胞的WHV复制也是静止的,但通常在脾脏中复制,并且外周血单核细胞的静态WHV可以通过脂多糖刺激在体外激活。我会。越来越多的研究也表明,从急性感染中回收的土拨鼠外周血单个核细胞带有感染性WHV DNA。总之,无论是从急性感染期还是从慢性感染土拨鼠中恢复过来,外周血单个核细胞的WHV感染状况都相似,在上述两种情况下,ConA,使用PHA和LPS。当受有丝分裂原刺激时,外周血单核细胞显着增加。淋巴系统的感染不会影响病毒触发的免疫反应。其实。不论急性或慢性WHV感染,均无因淋巴结肿大,淋巴细胞减少,淋巴瘤和全身免疫缺陷引起的机会性感染。与自然恢复的后果一样,慢性WHV的治疗应侧重于所有病毒库以及淋巴组织和肝脏中各种形式的复制。对自我限制型WHV的一项
研究显示了与自我限制型人HBV感染相关的各种免疫类型。一般而言,新生儿和成年土拨鼠的自限性感染具有以下特征:(1)在急性感染期间,在肝脏和血清中检测到病毒DNA和抗原高峰期;(2)针对抗原的快速细胞免疫反应;③急性病毒性肝炎但轻度肝损伤;④血清中转氨酶活性的短峰,随后恢复正常;⑤血清中出现病毒中和抗体,晴天在血液和肝脏中引起病毒和病毒抗原。恢复过程中对病毒抗原的体液免疫具有以下特征:在急性感染的发作和减少时(通常在实验室感染后的几周内)会产生高滴度的抗核心抗原抗体。以及具有中和和保护活性的抗表面抗原抗体。在成年土拨鼠中,细胞介导的免疫涉及激活外周血单核细胞。通过在体外用WHsAg,WHcAg和两种抗原的合成肽刺激外周血单核细胞已证实了这一点。外周血单核细胞对WHcAg的成功应答与血清中的病毒清除率有关,而病毒清除与WHcAg的几个重要抗原位点有关。与未免疫的土拨鼠相比,WHcAg抗原的主要表位区域(97-110个氨基酸)被用于免疫成年土拨鼠,WHV感染减弱了急性感染反应。在从急性感染中恢复期间,仍在研究外周血对WHsAg和WHXAg的反应。 在新生的土拨鼠WHV感染的急性期,无论使用何种病毒接种,其细胞免疫反应均与成年土拨鼠相似。健康的外周血单核细胞对病毒抗原的反应对于清除血清中的病毒DNA和WHsAg至关重要。对WHcAg引起的免疫反应的详细研究揭示了该抗原的几个特定表位。与成年土拨鼠感染相似,新生土拨鼠也会与WHcAg抗原的主要区域(氨基酸97-110,氨基酸100-113)反应。
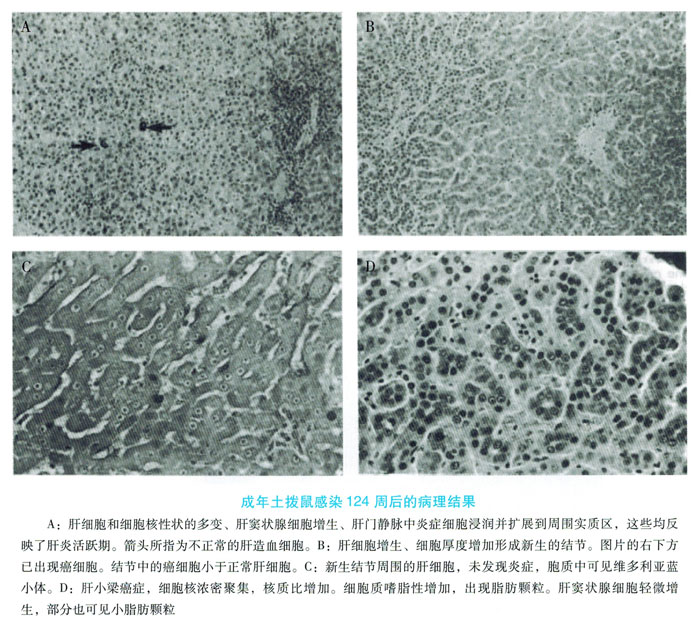
在肝脏中,成年自噬性伍德查克感染的自限性特征,包括轻度至明显的肝脏炎症和损害,CD3 + T细胞积聚以及肝细胞凋亡和再生。
(4)抗病毒药:土拨鼠乙型肝炎模型研究提供了多种因素,可影响病毒感染,复制和慢性感染。由于WHV和HBV DNA聚合酶具有相似的生化特性,因此可以将Woodchuck模型用于评估抗病毒药物。使用此模型,学者们正在评估众多核苷酸类似物药物和其他抗病毒化合物。在伍德查克模型中,我们发现使用抗病毒非芳基治疗6周后,该药物具有长期毒性,导致肝功能不足和乳酸性酸中毒。这种症状模仿了非芳烃疗法临床使用所引起的致命副作用,表明土拨鼠可用于乙肝抗病毒药的临床前评估。然而,在大规模的药物筛查中,土拨鼠难以操作,价格昂贵,并且仍然难以克服其自身难以传播的缺点。
肝炎家族的病毒在猪中很流行,被称为猪乙型肝炎病毒(SHBV)。乙型肝炎临床检测试剂盒(ELISA试剂盒),免疫组织化学和电子显微镜可以检测到SHBV。在检测受SHBV感染的猪中,有24.8%可以检测到HBsAg和抗HBsAg,但几乎无法检测到e抗原和e抗原抗体。通过免疫组织化学检测肝样品中的表面和核心抗原。肝实质区域中的细胞经历点状畸形和坏死,导致纤维结缔组织急剧增加。像HBV颗粒一样,透射电镜可以在肝细胞的核区域中看到,分为20m和40m颗粒,分别对应于HBV球形和Dane颗粒。
作为实验动物,猪比其他对HBV易感的动物具有无与伦比的优势。猪被广泛用于医学研究,并有良好的供应来源。因此,对猪乙型肝炎模型的详细研究将有助于促进HBV感染的病因和免疫学,并有望在将来成为更常见的HBV模型动物。