
传统三维单分子定位显微技术存在明显的分辨率各向异性,轴向分辨率远低于横向,难以清晰呈现细胞内部超微结构的立体形态,而能够实现各向同性纳米分辨率的双物镜4Pi-SMLM,又因仪器结构复杂、光路对准要求严苛、搭建与维护成本高昂,难以在普通生物实验室广泛应用,此前的单物镜简化干涉方案也存在相位稳定性差、易受环境振动与热漂移干扰的问题,无法兼顾高分辨率与实用性。西湖大学章永登特聘研究员研发了单物镜镜面增强4Pi‑SMLM技术,通过反射镜实现照明干涉,以极简结构实现各向同性纳米级定位精度与分辨率,成功用于细胞、活细胞及脑片的三维超分辨成像。相关内容以“Mirror-enhanced 4Pi-SMLM with one objective enables isotropic nanoscale imaging”为题发表在《Nature Biotechnology》上。

【主要内容】
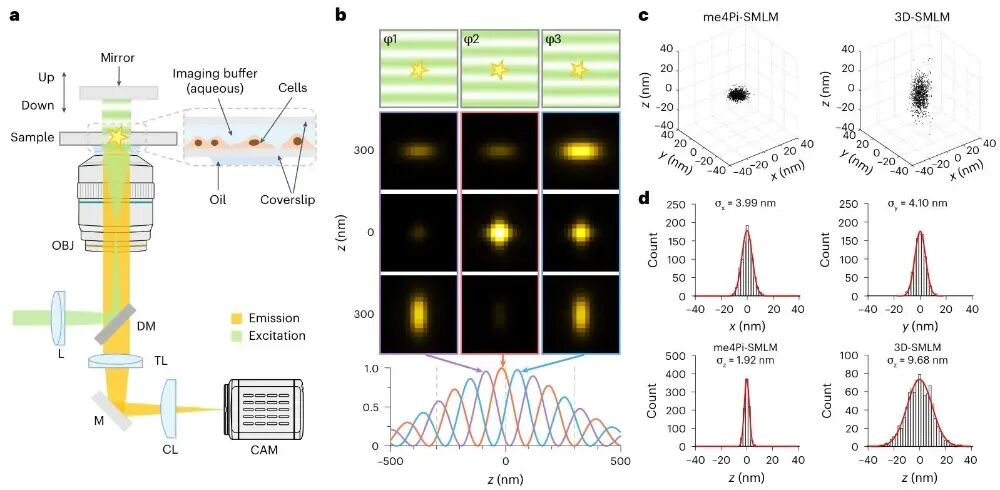
图1 me4PiSMLM的核心工作原理与系统可行性验证作者通过单物镜搭配反射镜形成轴向驻波干涉条纹,结合压电陶瓷驱动反射镜实现相位移动,并借助柱面镜引入像散完成轴向定位解模糊,同时以荧光微球为样品定量对比,证明该技术相比传统3DSMLM轴向定位精度提升约五倍,实现了2–3 nm的近各向同性定位精度。
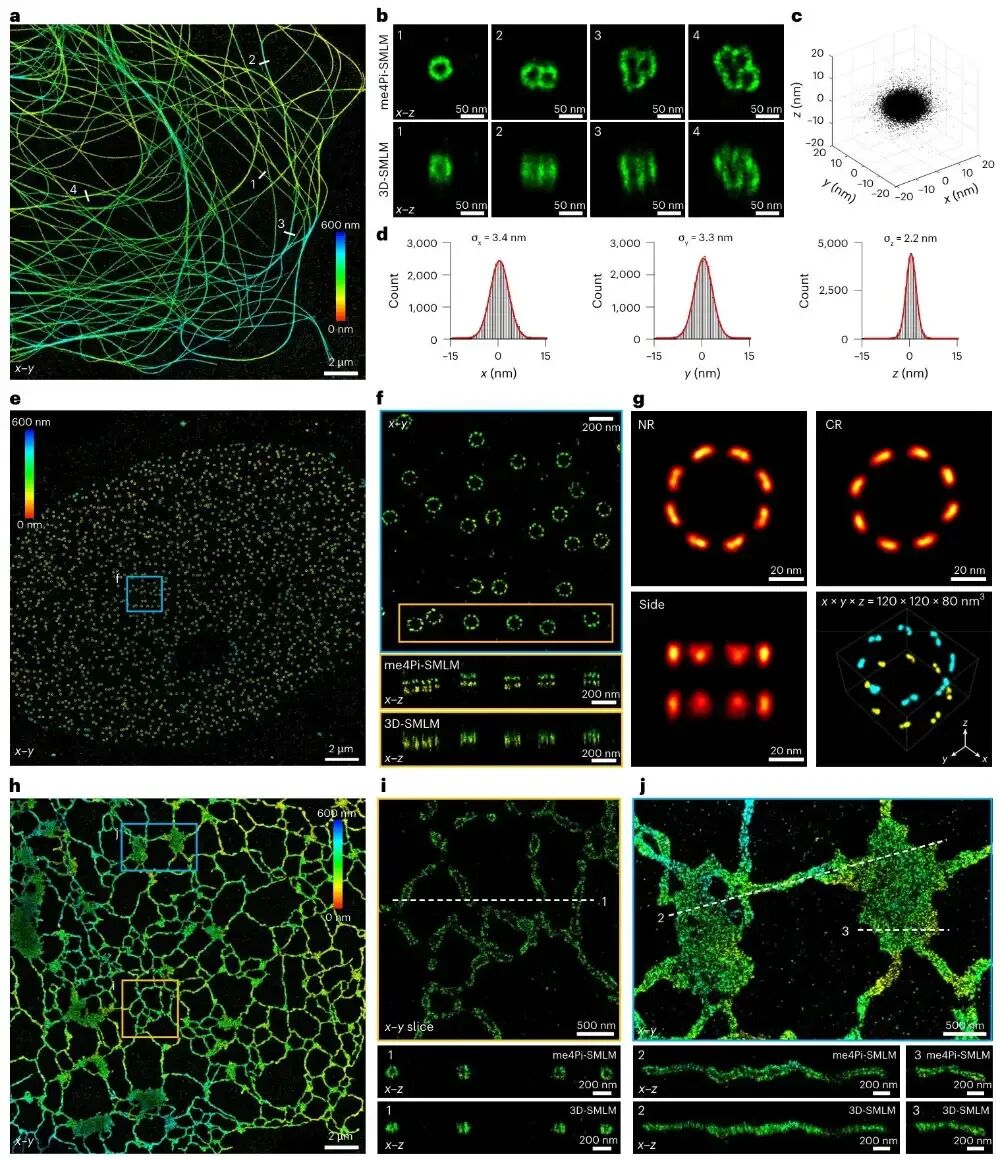
图2 me4PiSMLM在固定细胞样本中对亚细胞精细结构的解析能力me4PiSMLM成功清晰分辨COS7细胞中微管的中空环状结构、U2 OS细胞内核孔复合体Nup96的双层环状与对称亚基特征,以及内质网的管状与片状精细形态,各项定量分析显示其三维分辨率优于10 nm,远优于传统3DSMLM的成像效果。
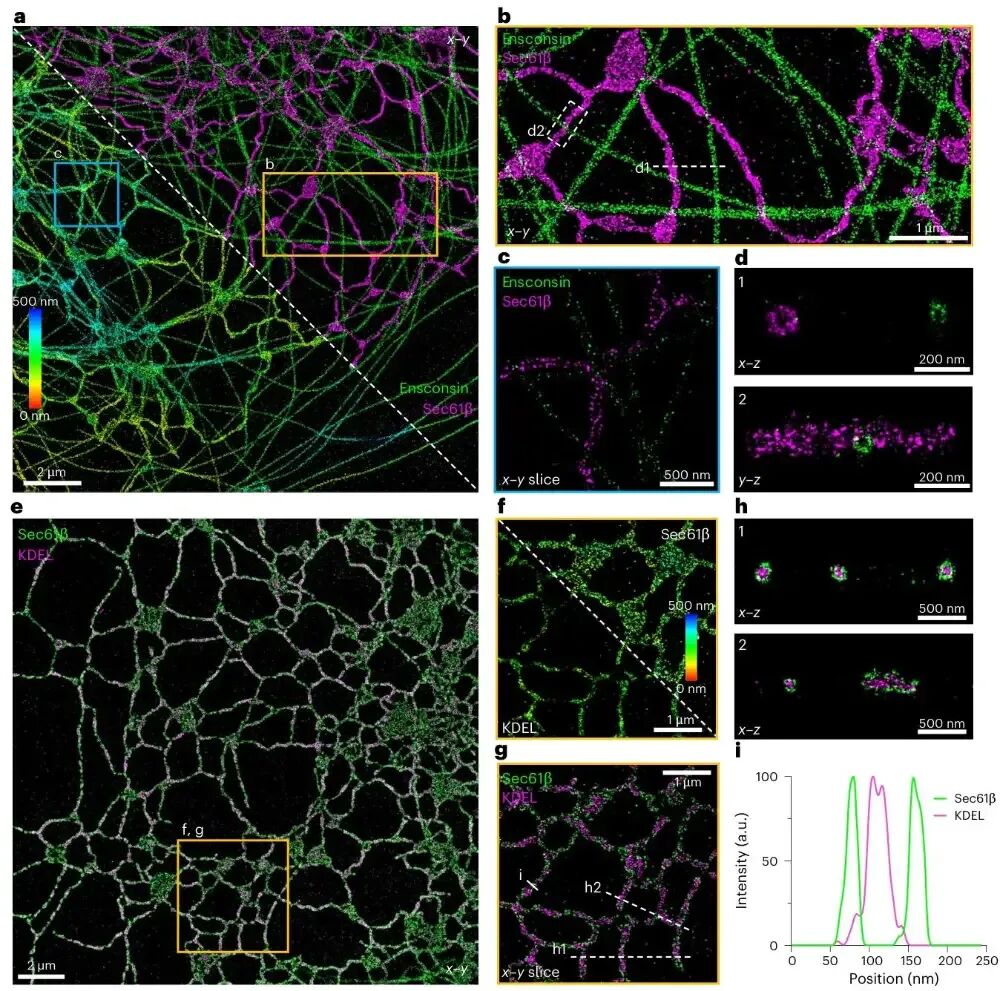
图3 me4PiSMLM的双色同步成像能力作者结合回收荧光技术实现两种荧光探针的高效光谱分离与低串扰成像,分别对细胞内微管与内质网、内质网膜与内腔进行双色标记成像,清晰呈现不同细胞器或结构间的空间位置关系与精细排布。
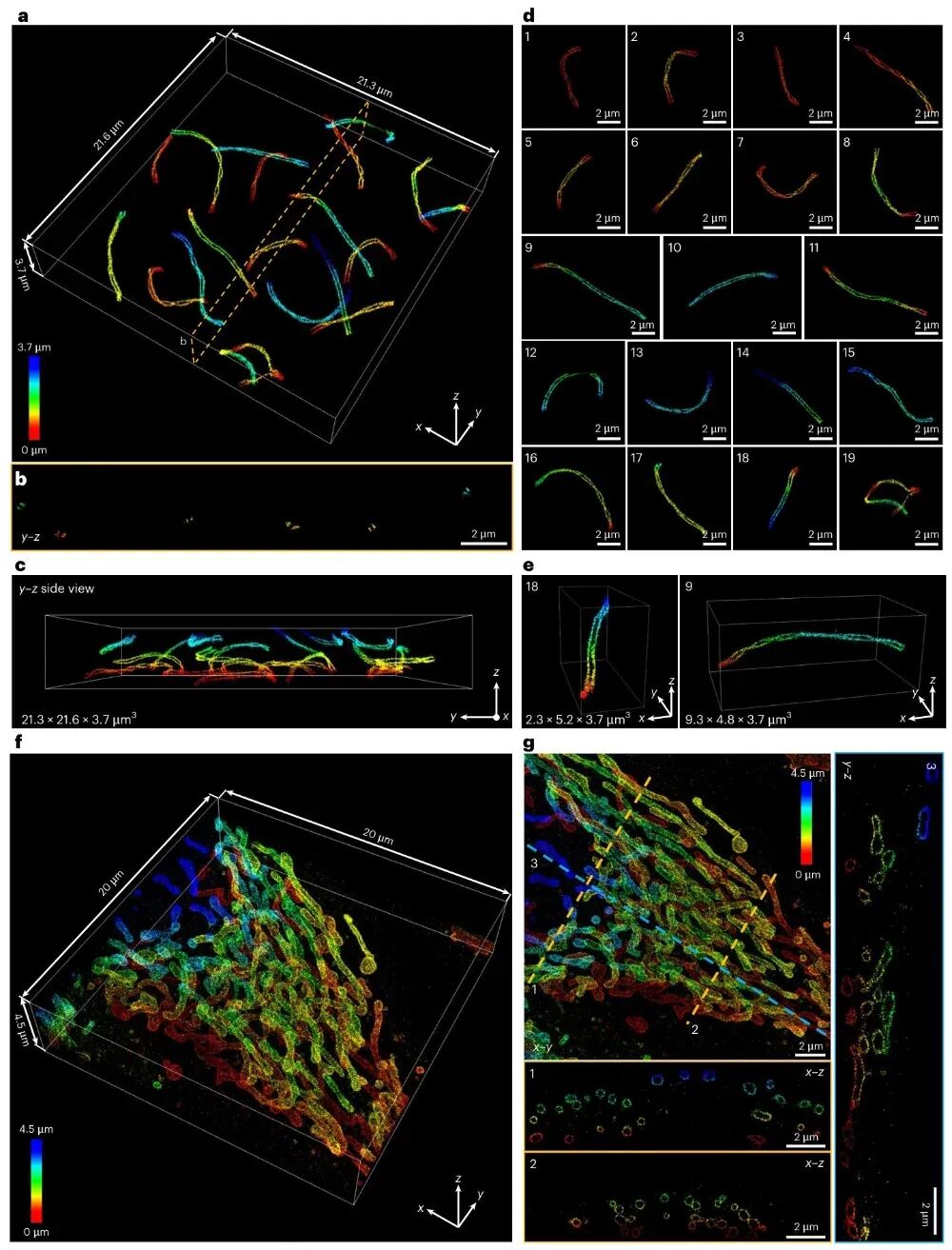
图4 me4PiSMLM的全细胞三维成像能力作者通过轴向层扫与图像拼接,成功对小鼠精母细胞联会复合体、HeLa细胞线粒体进行深度达数微米的全细胞三维重构,清晰呈现复杂超微结构的立体形态与空间分布,且在整个成像体积内保持稳定的高定位精度与分辨率,无明显伪影。
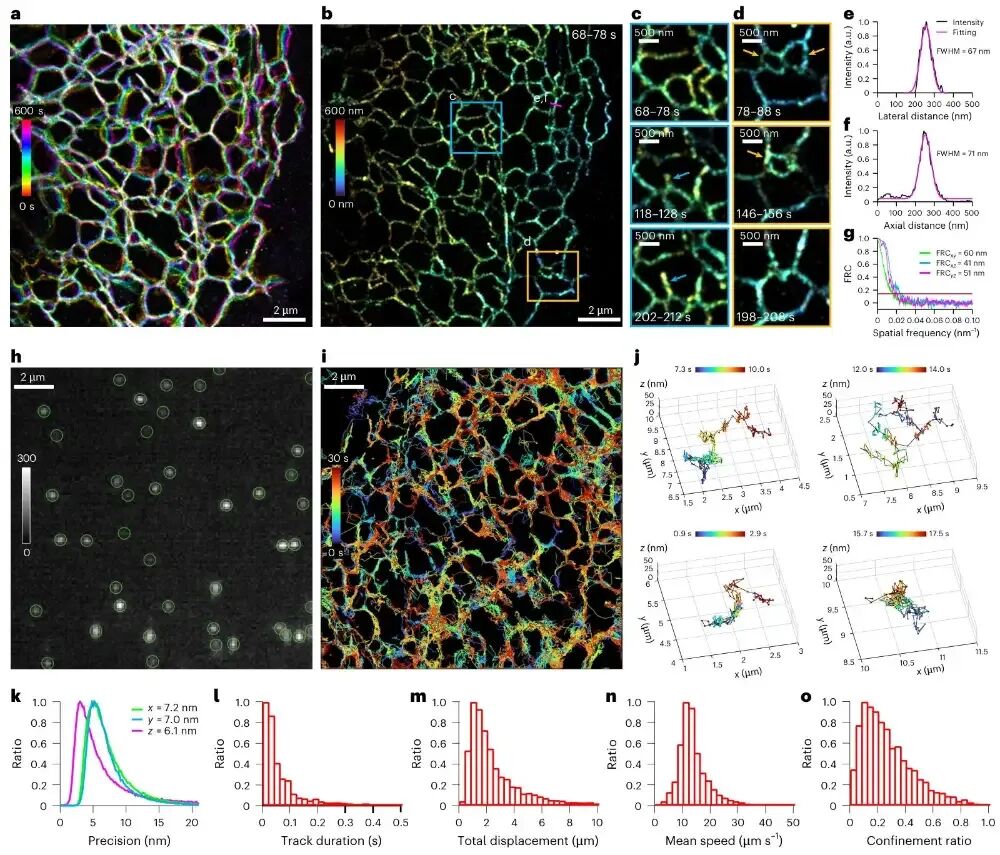
图5 me4PiSMLM在活细胞中的动态成像与单分子三维追踪me4Pi SMLM对活细胞内质网进行长时程三维超分辨观测,捕捉到内质网管状结构的生长、融合与消失等动态过程,同时完成单分子三维轨迹追踪与定量分析,获得6–7 nm的活细胞定位精度,填补了传统4PiSMLM难以用于活细胞成像的技术空白。
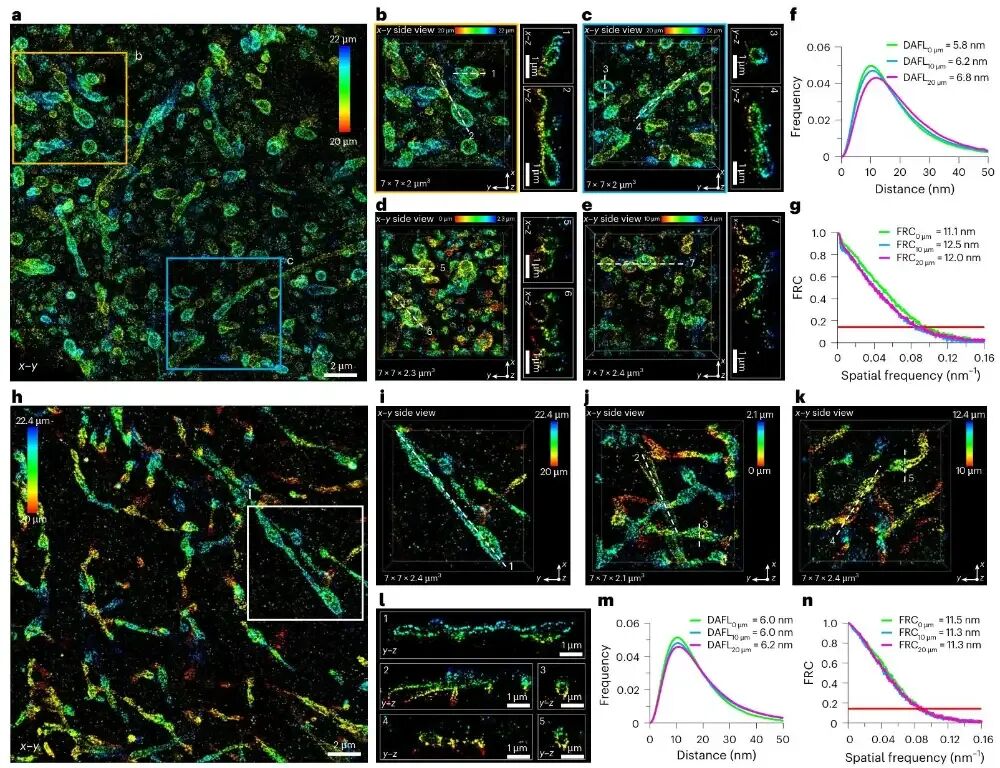
图6 me4PiSMLM应用于组织样本的纳米成像me4PiSMLM在30 μm厚的小鼠脑片中实现约20 μm深度的高质量成像,清晰分辨线粒体的形态特征与光敏感通道蛋白ChR2在轴突膜上的纳米级聚集分布,在组织环境中依然保持约6 nm的三维定位精度与优于15 nm的各向同性分辨率。【全文总结】这篇研究针对传统3D-SMLM轴向分辨率不足、双物镜4Pi-SMLM系统复杂难以普及的痛点,创建了单物镜镜面增强4Pi-SMLM(me4Pi-SMLM)新技术。研究通过多类生物样本验证,成功实现亚细胞结构超高分辨解析、双色成像、全细胞三维重构、活细胞动态与单分子追踪,并在小鼠脑片实现20 μm深度、15 nm以内各向同性分辨率的组织成像。